توضیحات
پروژه شبیه سازی باتری لیتیم یون(LiMn2O4) در نرم افزار انسیس فلوئنت(ANSYS FLUENT)
باتری:
باتری ها از ابزار ذخیرة انرژی هستند که انرژی شیمیایی ذخیره شده در مواد فعال الکترودها را به انرژی الکتریکی تبدیل می کنند. این قطعات شامل یک یا چند سلول می باشند که به طور سری یا موازی و یا هر دو حالت به هم متصل شده اند تا ولتاژ و ظرفیت مورد نیاز را بدست آورند. واکنش هایی که در سلول ها(باتری ها) اتفاق می افتند یک واکنش اکسایش – کاهش است. الکترود آند در سلول (باتری) اکسید می شود و الکترون آزاد می کند و الکترود کاتد الکترون ها را می گیرد و کاهش می یابد. وقتی دو الکترود از طریق یک مدار خارجی به یکدیگر متصل شوند واکنش به طور همزمان اتفاق می افتد و الکترونها در مدار خارجی شارش می یابند و جریانی را تولید می کنند که می تواند یک مقاومت بار در مدار را تغذیه کند. همزمان الکترولیت با انتقال یون ها بین مواد فعال الکترودها در واکنش شرکت می کند.
براساس برگشت پذیر بودن فرآیندهای الکتروشیمیایی، باتری ها به دو دسته باتری های اولیه و ثانویه تقسیم می شوند:
١- باتری های اولیه نوعی از پیکربندی خاص سلولی هستند که در آنها واکنش های الکتروشیمیایی برگشت پذیر نیستند. این باتری ها غیر قابل شارژ می باشند و پس از مصرف انرژی دور انداخته می شوند.
۲- باتری های ثانویه، قابل شارژ می باشند و می توانند در یک بازه طولانی، چندین بار شارژ و دشارژ شوند. به منظور شارژ مجدد این نوع از باتری ها، یک منبع تغذیه الکتریکی خارجی با ولتاژ بالاتر از ولتاژ باتری لازم است. این باتری های نسبت به باتری های اولیه از نظر زیستی مناسب تر هستند. این باتری ها کاربردهای گسترده – ای در مصارف خانگی، ابزار بدون سیم (مثل دریل و آچار)، قطعات ارتباطی قابل حمل و کامپیوترهای قابل حمل دارند. آنها همچنین کاربردهای صنعتی شامل کاربردهای فضایی، نظامی (مثل پرتاب کننده ها، موشک ها و ماهواره ها) و ترابری وسایل نقلیه الکتریکی و الکتریکی هیبریدی دارند. چندین نوع مختلف از باتری های قابل شارژ تجاری شده وجود دارند. رایج ترین آنها عبارتند از: باتری سرب -اسیدی، نیکل-کادمیوم، هیبرید فلز-نیکل، یون لیتیومی، پلیمری یون لیتیومی و قلیایی قابل استفاده مجدد.
باتری لیتیوم یون:
سلول باتری لیتیوم یونی به طور معمول از الکترود مثبت، الکترود منفی، الکترولیت، جداساز، جمع کننده جریان و پوسته تشکیل شده است. شکل زیر نمایی از یک سلول باتری لیتیوم یون معمولی را نشان می دهد. الکترودها اجزای کلیدی داخل سلول هستند که ظرفیت و چگالی انرژی باتری را تعیین می کنند. باتری های لیتیوم یون یکی از انواع باتری های ثانویه هستند باتری هایی که قابلیت شارژ شدن مجدد را دارند. در این نوع باتری یون لیتیوم بین آند و کاتد حرکت می کند. کاتد معمولاً از یک اکسید فلزی و آند از یک ماده کربنی ساخته می شود و هر دو الکترود متخلخل هستند. الکترولیت از یک محلول آلی و نمک لیتیوم تشکیل می شود. بین آند و کاتدیک ورقه متخلخل(جداکننده ) قرار دارد که از اتصال مستقیم آنها جلوگیری می کند. همچنین مواد فعال هر الکترود بر روی زیرلایه ای فلزی قرار دارند که جمع کننده نامیده می شود و وظیفه آن جمع آوری الکترونها می باشد. شکل زیر یک باتری استوانه ای لیتیوم یون را نشان می دهد. لایه های نازک آند، کاتد و جداکننده حول یک محور مرکزی لوله شده اند و درون یک قوطی استوانه ای قرار گرفته اند. فضای خالی هم با الکترولیت مایع پر شده است.
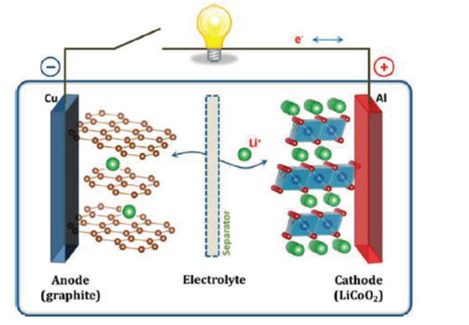
شکل نمای یک سلول باتری لیتیوم یونی.
در باتری لیتیوم یونی، بار الکتریکی در سیال توسط یون لیتیوم و در جامد توسط الکترون ها حمل می شود. همانگونه که در شکل فوق نشان داده شده است، جهت جریان یون ها طی فرایند شارژ از الکترود مثبت به الکترود منفی و در فرایند دشارژ برعکس می باشد. یون ها کوچک هستند و حین فرایند شارژ از مواد فعال موجود در الکترود مثبت خارج شده و به درون ساختار مواد فعال الکترود منفی نفوذ می کنند.
ویژگی های باتری های لیتیوم یونی:
خصوصیات برجسته باتری های لیتیوم یونی عبارتند از:
1- ولتاژ عمل بالا: پتانسیل کارکردی میانگین یک تک سلول، تقریبا 3.6 ولت است که سه برابر ولتاژ عملکردی باتری های نیکل کادمیوم و حدود دو برابر باتری های سرب اسیدی است.
۲- متراکم، سبک وزن و چگالی بالا: چگالی انرژی آن در حدود 1.5 برابر و انرژی مخصوصش در حدود دو برابر باتری های نیکل کادمیوم است.
٣- پتانسیل شارژ سریع: این باتری ها می توانند با یک ساعت شارژ سریع حدود ۸۰-۹۰٪ از کل ظرفیت را به دست آورند.
۴- سرعت دشارژ زیاد: تا 3C (سه برابر ظرفیت) قابل تحمل است.
۵- ناحیه وسیع دمای عملکردی
۶- دشارژ خود به خودی بسیار کم: فقط ۱۲-۸٪ در ماه
۷- طول عمر: بالغ بر ۵ سال به تعمیر نیاز ندارد.
۸- اثر حافظه ای : دوباره تا ولتاژهای موردنظر اولیه شارژ و تخلیه می شود.
ظرفیت باتری: معادل مقدار باری است که می تواند آزاد کند. ظرفیت نظری یک ماده فعال از رابطه زیر محاسبه می شود:
که در آن M جرم مولی ماده فعال، x تعداد الکترون واردشده به ازای هر مول ماده فعال و F ثابت فارادی(coulomb/mol 96486) می باشند.
انرژی ویژه: مقدار انرژی ذخیره شده در سیستم موردنظر در واحد جرم می باشد.
توان ویژه با چگالی توان: برابر مقدار توانی است که باتری آزاد می کند.
عمر چرخه ای: تعداد چرخه ای است که باتری می تواند شارژ و دشارژ شود تا زمانی که ظرفیت دشارژ به ۸۰% ظرفیت دشارژ اولیه برسد.
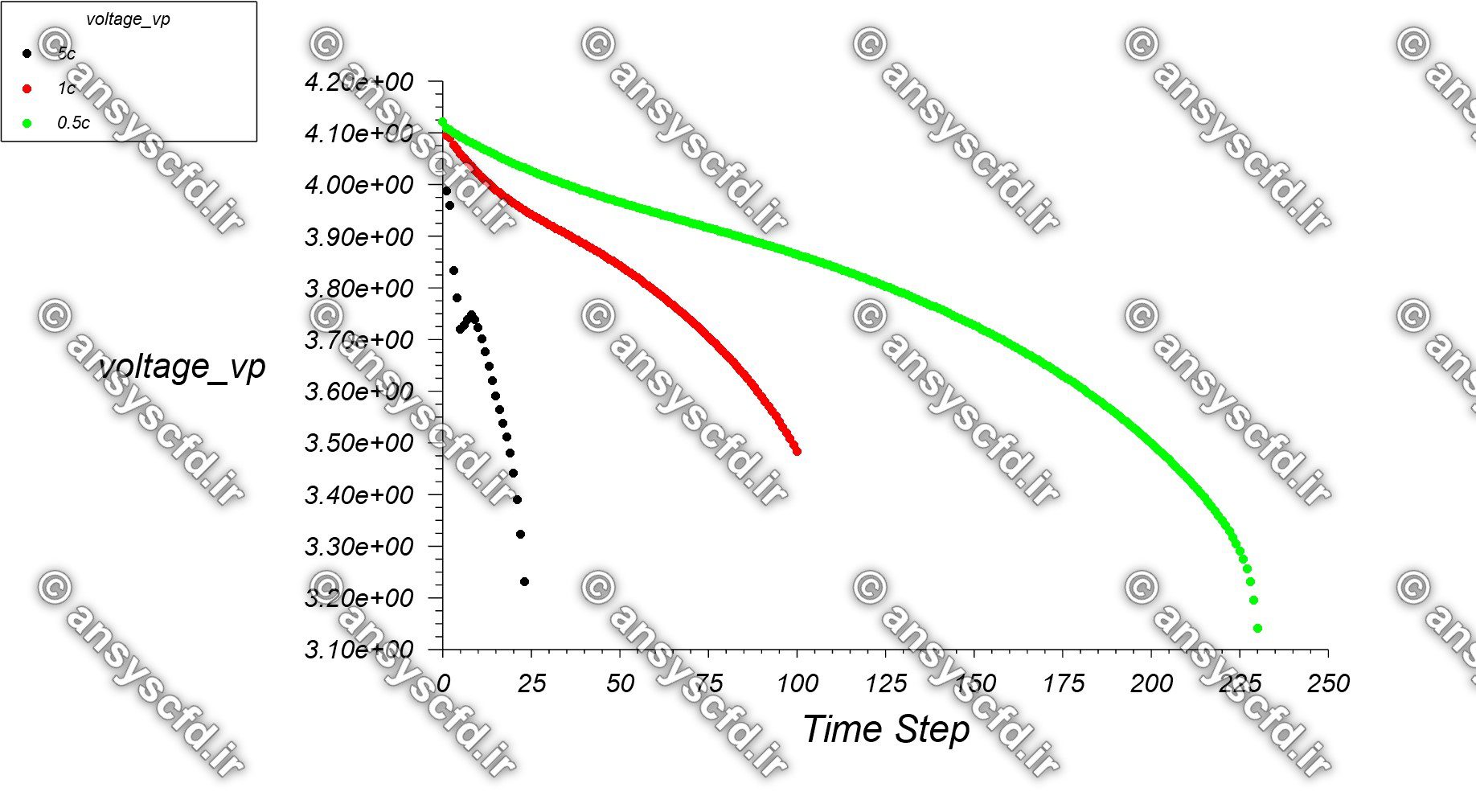
C-rate: جریان باتری برحسب C-rate بیان می شود. C-rate معادل آهنگی است که باتری نسبت به بیشترین مقدار ظرفیتش، دشارژ می شود. نرخ ۱C معادل جریانی است که در آن، باتری در ۱ ساعت دشارژ می شود. برای باتری با ظرفیت Ah ۱۰۰، نرخ ۱C با جریان دشارژ A ۱۰۰، نرخ ۵C با جریان دشارژ A ۵۰۰ و نرخ C/2 با 50 A معادل می باشد.
شرح پروژه:
در این پروژه شبیه سازی باتری لیتیم یون(LiMn2O4) در نرم افزار انسیس فلوئنت(ANSYS FLUENT) انجام شده است.
هندسه مسئله:
هندسه مسئله در نرم افزار انسیس دیزاین مدلر(ANSYS Design Modeler) ترسیم شده است.
شبکه و مش:
شبکه و مش در نرم افزار انسیس مشینگ(ANSYS Meshing) تولید شده است.
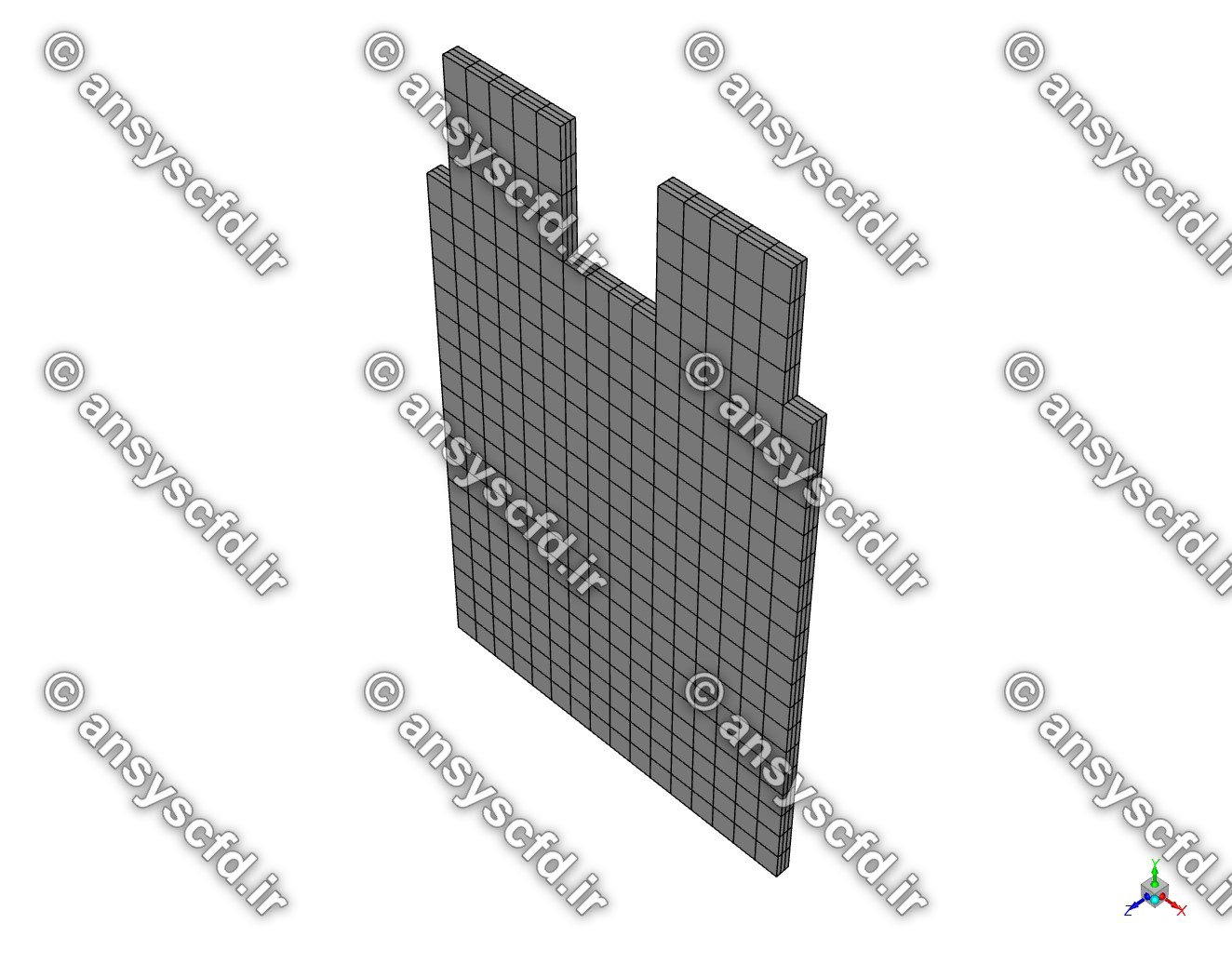
شبیه سازی و حل:
شبیه سازی در نرم افزار انسیس فلوئنت(ANSYS FLUENT) انجام شده است.
حلگر:
حلگر فشار مبنا (Pressure based) در شرایط گذرا استفاده شده است.
مدل باتری:
مدل باتری MSMD و NTGK استفاده شده است.
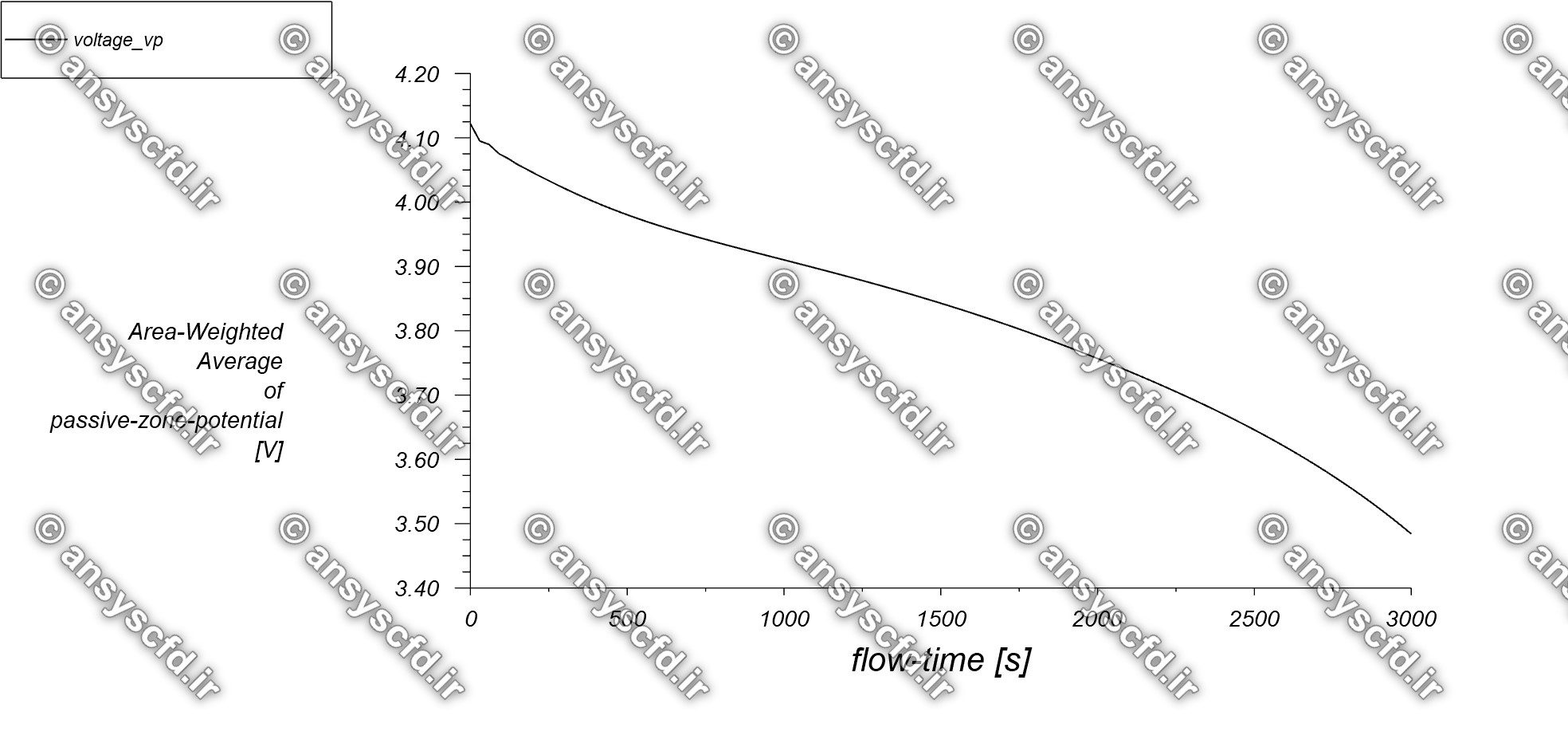
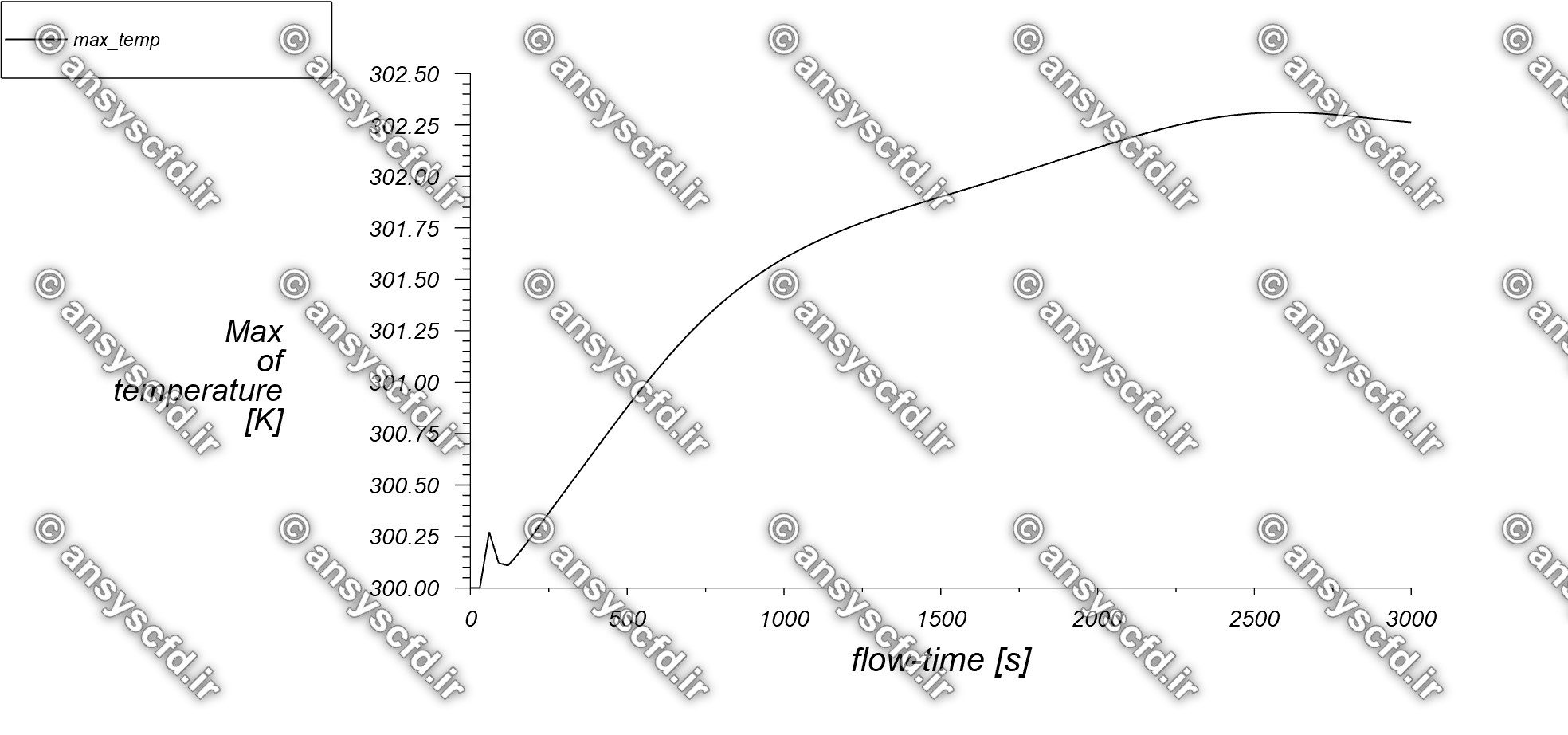
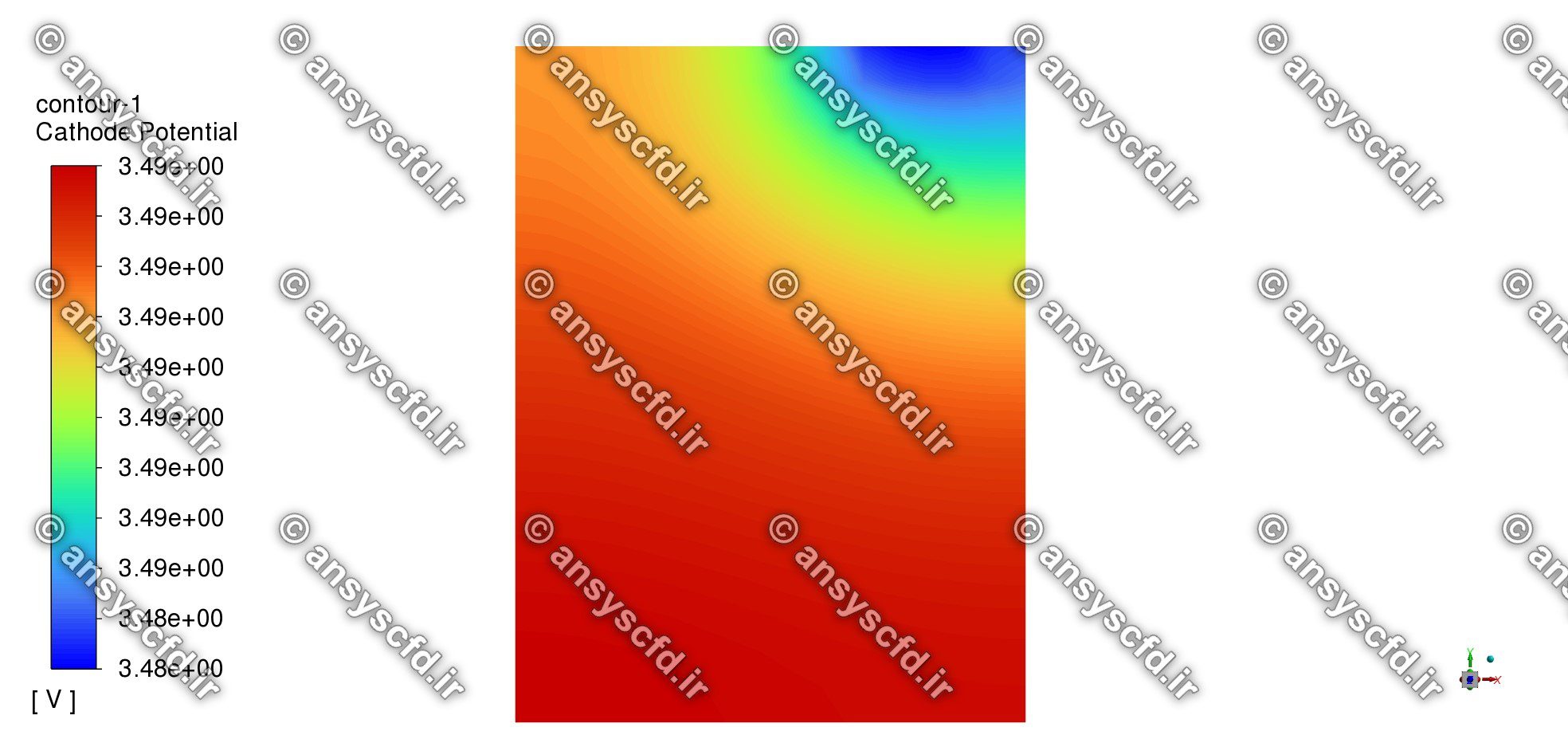
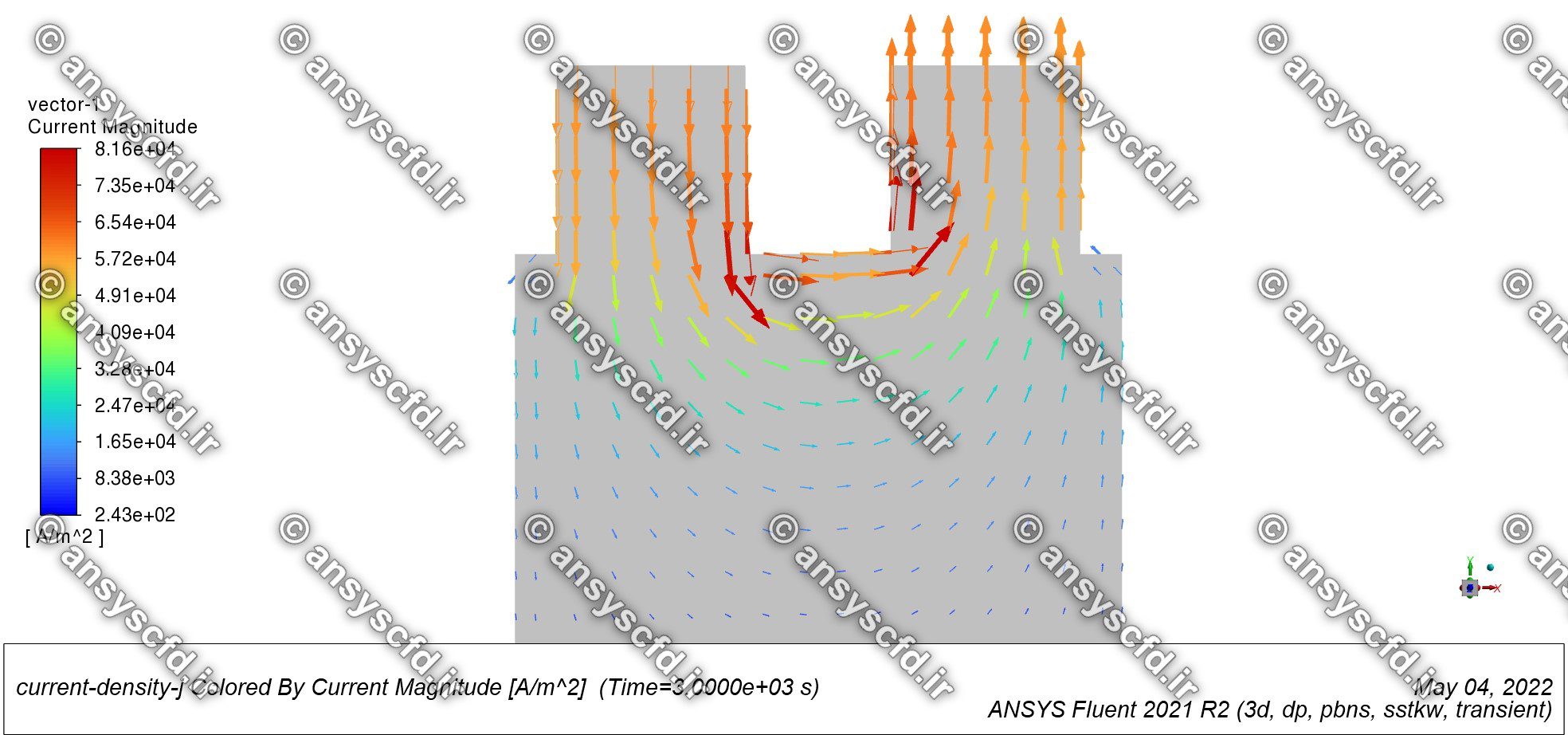
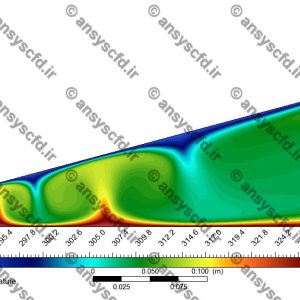
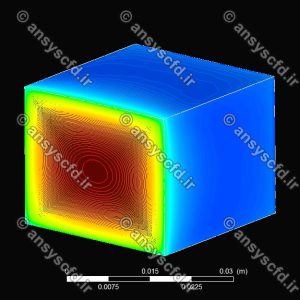
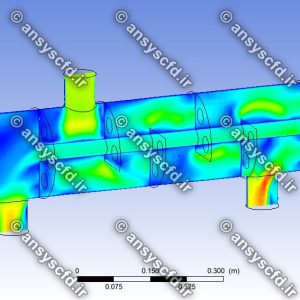
نمونه نتایج شبیه سازی: